En una entrada anterior informábamos que cerca de la mitad de los casos de discapacidad intelectual permanecen sin diagnostico etiológico y que se estima que un 40% tienen origen genético. Por su mayor frecuencia destaca la trisomía 21 y el síndrome de X frágil. Sin embargo, la casuística es muy amplia y en la plataforma de genes y fenotipos relacionados con la discapacidad intelectual Orphanet y ERN ITHACA podemos encontrar 979 enfermedades genéticas raras que cursan con discapacidad intelectual.
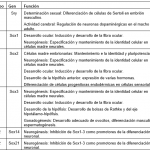
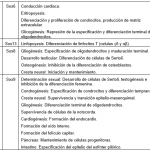
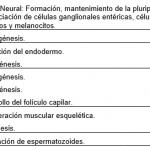
Las proteínas SOX pertenecen a la familia de los factores de transcripción (Tfs) poseyendo un dominio de unión al ADN de la clase HMG. Se codifican desde los genes Sox y tienen funciones en el desarrollo de órganos y destino celular. En Leon, A. (2019) podemos encontrar el grupo y las funciones de cada uno de los genes Sox (1).
 |
 |
 |
 |
(Clic para ampliar las imágenes)
Por su parte Stevanovic et al. (2021) proporcionan una síntesis de sus implicaciones para el desarrollo del sistema nervioso y la neurogénesis adulta y la localización de cada gen (2).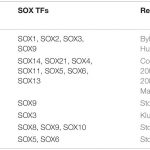
(Clic para ampliar la imagen)
Dada su implicación en la configuración del SN no es de extrañar que alteraciones genéticas en ellos puedan conllevar discapacidad intelectual. El ya citado trabajo de Stevanovic et al. (2021) proporciona un resumen de las variantes asociadas a trastornos del neurodesarrollo (Tabla suplementaria S1). En Underwood et al., podemos encontrar un revisión de las variantes y fenotipos asociados (3).
1.- Leon, A. (2020). Historia evolutiva de los genes sox durante el proceso de duplicación genética. REBIOL, 39(2), 58-69. Recuperado a partir de https://revistas.unitru.edu.pe/index.php/facccbiol/article/view/2734
2.- Stevanovic M, Drakulic D, Lazic A, Stanisavljevic Ninkovic D, Schwirtlich M and Mojsin M (2021) SOX Transcription Factors as Important Regulators of Neuronal and Glial Differentiation During Nervous System Development and Adult Neurogenesis. Front. Mol. Neurosci. 14:654031. doi: 10.3389/fnmol.2021.654031.
https://www.frontiersin.org/articles/10.3389/fnmol.2021.654031/full
3.- Underwood, A.; Rasicci,D.T.; Hinds, D.; Mitchell, J.T.; Zieba,J.K.; Mills, J.; Arnold, N.E.; Cook,T.W.; Moustaqil, M.; Gambin, Y.; et al.Evolutionary Landscape of SOXGenes to Inform Genotype-to-Phenotype Relationships.Genes2023,14, 222. https://doi.org/10.3390/genes14010222
